




模塊化合成是現(xiàn)代有機(jī)合成的重要理念,先平行合成一系列結(jié)構(gòu)明確的小分子“構(gòu)建單元”,再像搭積木一樣將它們高效、可預(yù)測(cè)地組裝成復(fù)雜目標(biāo)分子。有機(jī)硼試劑因其制備簡(jiǎn)便、穩(wěn)定性高、反應(yīng)多樣,成為模塊化合成的理想工具。Burke利用雙功能MIDA硼酸鹽(MIDA = N-甲基亞氨基二乙酸酯)的Suzuki-Miyaura反應(yīng)實(shí)現(xiàn)了對(duì)富含C(sp2)分子的模塊化合成(圖1a),這項(xiàng)工作也被擴(kuò)展為一個(gè)自動(dòng)化的“分子打印機(jī)”,能夠制備數(shù)百種不同的目標(biāo)分子。雖然Burke、Suginome、Aggarwal等人已在C(sp2)–C(sp2)偶聯(lián)和C(sp3)鏈擴(kuò)展方面取得重要進(jìn)展,但C(sp3)–C(sp3)鍵的立體特異性構(gòu)建仍極具挑戰(zhàn)。
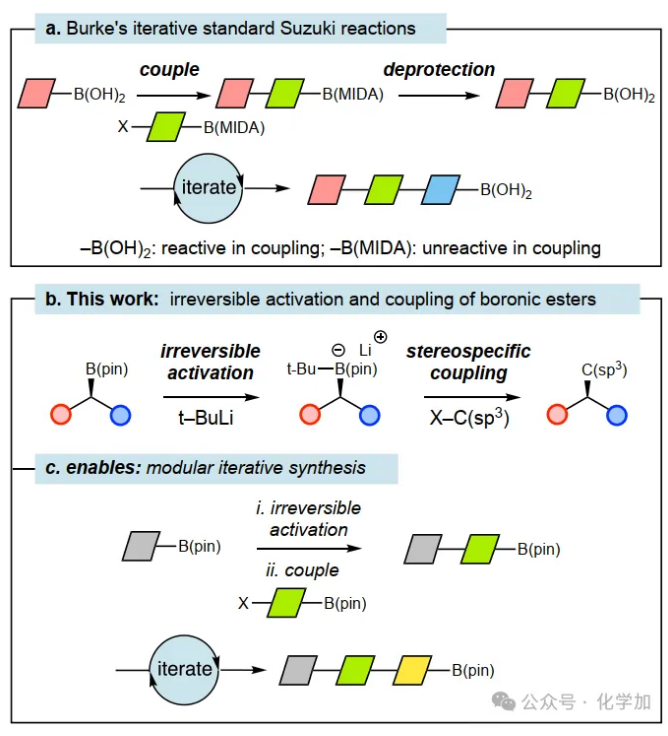
圖1. 背景介紹及本文的工作(圖片來(lái)源:Nature)
本文中,James P. Morken教授課題組介紹了一種立體專一性C(sp3)-C(sp3)交叉偶聯(lián)的方法,其通過(guò)不可逆地活化仲烷基硼酸酯,隨后與一個(gè)非活化的脂肪族親電試劑進(jìn)行偶聯(lián)(圖1b)來(lái)實(shí)現(xiàn)。由于活化是不可逆的,并且在加入親電試劑之前完成,這種交叉偶聯(lián)模式為模塊化和迭代合成提供了另一種途徑(圖1c)。活化后,將活化的硼酸酯與含有B(pin)的親電試劑進(jìn)行化學(xué)選擇性偶聯(lián),將生成一個(gè)含有硼的新片段,為下一輪活化和偶聯(lián)做好準(zhǔn)備。該方法可以在合成過(guò)程中使用大的、具有多樣化官能團(tuán)的構(gòu)建模塊,最終實(shí)現(xiàn)復(fù)雜目標(biāo)的簡(jiǎn)短合成。
在上述合成策略中,形成C(sp3)-C(sp3)鍵所需的交叉偶聯(lián)仍然是有機(jī)合成中的重大挑戰(zhàn)。盡管在外消旋親核試劑和親電試劑之間對(duì)映匯聚式偶聯(lián)的開(kāi)發(fā)方面已取得實(shí)質(zhì)性進(jìn)展(圖2a),但當(dāng)?shù)孜镌谇笆中苑磻?yīng)中心帶有相似的取代基(R1和R2)時(shí),要實(shí)現(xiàn)高選擇性仍然罕見(jiàn),從而限制了這些反應(yīng)的底物范圍。對(duì)映專一性交叉偶聯(lián)提供了一種替代方法:只要能夠獲得富含對(duì)映體富集的起始原料,并且轉(zhuǎn)化是立體專一的,那么最終產(chǎn)物的立體化學(xué)就可以預(yù)先確定。用叔丁基鋰活化對(duì)映體富集的硼酸酯形成的四配位硼“ate”絡(luò)合物,可以通過(guò)立體專一的轉(zhuǎn)金屬化與銅和鋅鹽反應(yīng),從而能夠與一系列高反應(yīng)活性親電試劑(烯丙基、炔丙基、酰基等)進(jìn)行偶聯(lián)。作者認(rèn)為,如果硼酸酯能夠與非活化的脂肪族親電試劑偶聯(lián),特別是當(dāng)該親電試劑含有另一個(gè)硼酸酯時(shí),烷基鋰活化方法可能有助于模塊化合成。本文中,在適當(dāng)?shù)臈l件下,實(shí)現(xiàn)了一種銅-乙炔絡(luò)合物通過(guò)催化對(duì)映體富集的仲硼酸酯與未官能化烷基親電試劑之間的C(sp3)-C(sp3)偶聯(lián),并且可用在復(fù)雜分子合成中。化學(xué)加,加你更精彩。
對(duì)C(sp3)-C(sp3)偶聯(lián)反應(yīng)的研究采用了叔丁基鋰活化的仲烷基硼酸酯1,該化合物可方便地制備為固體材料,在惰性氣氛下儲(chǔ)存>6個(gè)月不會(huì)降解(圖2b)。在25 °C下,底物1、CuCN和CH3I反應(yīng),以80%的產(chǎn)率得到偶聯(lián)產(chǎn)物2。最終確定,銅-乙炔絡(luò)合物與烷基對(duì)三氟甲基苯磺酸酯(OTsF)親電試劑具有良好的反應(yīng)活性,即使反應(yīng)中使用20 mol%的銅絡(luò)合物。在這些絡(luò)合物中,三異丙基硅基乙炔基配體提供了優(yōu)異的反應(yīng)活性(圖2e),推測(cè)是因?yàn)榕潴w骨架的位阻抑制了已知的通過(guò)橋連π絡(luò)合物進(jìn)行的催化劑寡聚化。
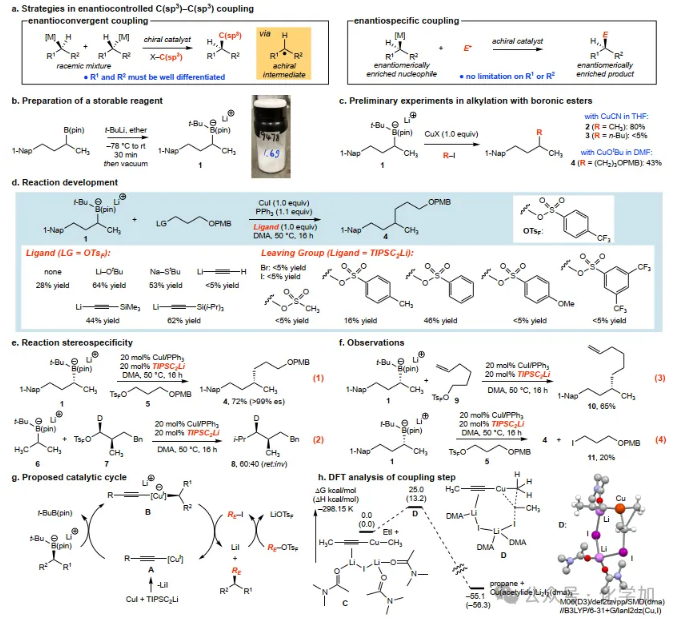
圖2. 催化C-C鍵形成方法及立體特異性C(sp3)-C(sp3)交叉偶聯(lián)反應(yīng)的開(kāi)發(fā)(圖片來(lái)源:Nature)
為了確定上述銅催化偶聯(lián)是否通過(guò)與其他銅基反應(yīng)相似的機(jī)制進(jìn)行,作者考察了該過(guò)程的立體專一性。如圖2e所示,硼“ate”絡(luò)合物1與親電試劑5之間的反應(yīng),在親核試劑方面表現(xiàn)出高水平的立體專一性(構(gòu)型保持>99%),這表明了類似于其他銅催化反應(yīng)的“內(nèi)球”轉(zhuǎn)金屬化機(jī)制。控制實(shí)驗(yàn)結(jié)合上文觀察到的碘甲烷的偶聯(lián)能力,該反應(yīng)按照?qǐng)D2g所示的過(guò)程進(jìn)行。原位生成的炔基銅絡(luò)合物A與活化的硼酸酯發(fā)生轉(zhuǎn)金屬化生成B,然后與推測(cè)是原位生成的碘代烷烴衍生物的親電試劑偶聯(lián)。碘代烷烴的生成很可能發(fā)生在磺酸酯被取代時(shí)伴隨構(gòu)型翻轉(zhuǎn),因此觀察到的親電試劑反應(yīng)凈構(gòu)型保持是雙重翻轉(zhuǎn)的結(jié)果。立體專一性的明顯缺失,推測(cè)是由于反應(yīng)過(guò)程中已知的碘代烷烴與游離碘化物的退行性SN2反應(yīng)所致。通過(guò)DFT計(jì)算了一條從假設(shè)的甲基(炔基)銅酸鹽(C)和碘乙烷生成烷基化產(chǎn)物的途徑(圖2h)。與Nakamura的計(jì)算一致,發(fā)現(xiàn)一當(dāng)量的碘化鋰促進(jìn)了該反應(yīng),它在一個(gè)涉及銅中心(D)但不經(jīng)過(guò)離散Cu(III)中間體的直接取代反應(yīng)中活化親電試劑,而這種Cu(III)中間體在其他Cu(I)與鹵代烷的反應(yīng)中已被檢測(cè)到。這種與已知反應(yīng)性的微妙偏離可能源于炔基配體的π-酸性,其足以降低還原消除的能壘,使得該步驟與氧化加成的發(fā)生同步進(jìn)行。
在研究催化偶聯(lián)的范圍時(shí)(圖3),發(fā)現(xiàn)多種活化的仲烷基硼酸酯都能參與反應(yīng)。該反應(yīng)也能耐受吡啶基團(tuán)(17),這對(duì)藥物合成具有重要意義。反應(yīng)在包含β-和γ-支鏈的硼酸酯(15,16)中也能良好進(jìn)行,以中等產(chǎn)率和高立體專一性提供產(chǎn)物。最引人注目的例子是化合物22的構(gòu)建:由于缺乏近端導(dǎo)向基團(tuán),該化合物難以通過(guò)手性匯聚偶聯(lián)反應(yīng)制備。然而,通過(guò)當(dāng)前的方法,可以以高立體專一性(ds>20:1)和高產(chǎn)率(81%)獲得該產(chǎn)物,為烷基化碳環(huán)化合物提供了一種有用的方法。該反應(yīng)還顯示出對(duì)親電試劑中一系列官能團(tuán)的耐受性,包括烯烴(25)、保護(hù)的炔烴(26)、烷基氯化物和氟化物(27,28)、芳基氯化物(29)和噻吩(30)。與使用格氏試劑的既定SN2型反應(yīng)相比,這些反應(yīng)條件更溫和,并且與堿敏感官能團(tuán)(如酯、腈和環(huán)氧化物)兼容(34-36)。與β-支鏈親電試劑的偶聯(lián)存在挑戰(zhàn),可能是由于位阻。為了解決這個(gè)問(wèn)題(31,32),炔化物配體被芳基(衍生自PhLi)取代,后者是更強(qiáng)的σ供體。該反應(yīng)對(duì)未活化的硼酸酯(Bpin)官能團(tuán)表現(xiàn)出惰性,這為迭代合成策略開(kāi)辟了可能性,通過(guò)化學(xué)選擇性偶聯(lián),從含有末端Bpin官能團(tuán)的片段構(gòu)建復(fù)雜的分子。
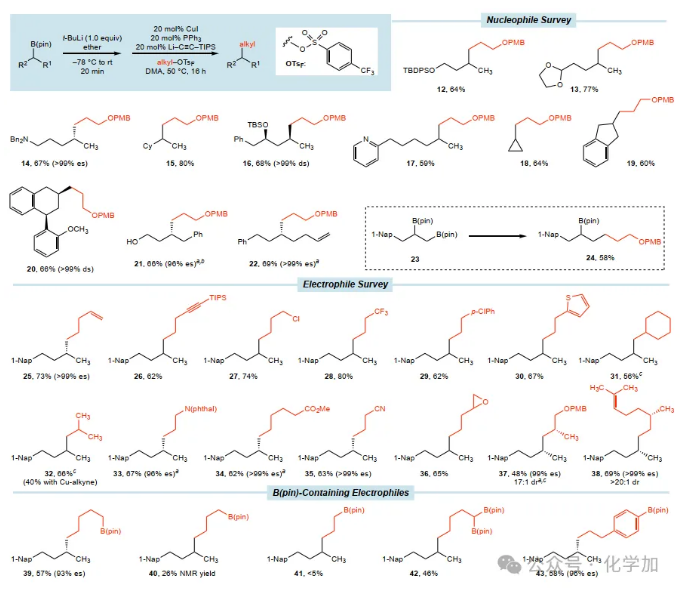
圖3. Cu催化的硼酸酯烷基-烷基交叉偶聯(lián)的范圍(圖片來(lái)源:Nature)
為了展示該反應(yīng)在復(fù)雜分子模塊化合成中的潛力,如圖4a所示,從易于獲得的Bpin官能化片段44開(kāi)始,與叔丁基鋰反應(yīng)得到活化的硼酸酯絡(luò)合物,然后與另一個(gè)Bpin功能化親電試劑進(jìn)行立體專一性偶聯(lián),得到含有C(sp3)-C(sp3)鍵的片段。然后重復(fù)這個(gè)序列,得到含有四個(gè)C-C鍵的低聚物(47),證明了該方法的迭代潛力。接下來(lái),展示了該反應(yīng)如何在兩個(gè)具有挑戰(zhàn)性的天然產(chǎn)物合成中實(shí)現(xiàn)關(guān)鍵的C-C鍵構(gòu)建。對(duì)于fluvirucinine A1的碳骨架合成,從仲烷基硼酸酯(48)開(kāi)始,它與親電試劑5偶聯(lián)得到49。末端烯烴然后通過(guò)一鍋兩步凈硼氫化反應(yīng)進(jìn)行硼化,得到50。與51偶聯(lián)得到中間體52,其包含構(gòu)建該天然產(chǎn)物所需的整個(gè)碳鏈和手性元素。對(duì)于(-)-spongidepsin的合成,從仲烷基硼酸酯53開(kāi)始,與含有遠(yuǎn)端硼酸酯的烷基親電試劑(54)偶聯(lián)得到55。單碳同系化和硼酸酯的氧化得到56,其通過(guò)與57形成酰胺鍵、選擇性脫除硅醚保護(hù)、內(nèi)酯化和脫炔基保護(hù)轉(zhuǎn)化為spongidepsin。

圖4. 立體特異性烷基-烷基交叉偶聯(lián)在化學(xué)合成中的應(yīng)用(圖片來(lái)源:Nature)
總結(jié)
James P. Morken教授課題組首次實(shí)現(xiàn)了銅催化的、手性仲烷基硼酸酯與非活化烷基親電試劑之間的立體專一性C(sp3)-C(sp3)交叉偶聯(lián),填補(bǔ)了該領(lǐng)域長(zhǎng)期存在的空白,為烷基-烷基鍵的立體可控構(gòu)建提供了全新工具,為復(fù)雜分子的合成提供了高效的模塊化和迭代方法。本文巧妙地將硼化學(xué)的模塊化優(yōu)勢(shì)與銅催化的獨(dú)特反應(yīng)性相結(jié)合,成功打通了立體專一性烷基-烷基偶聯(lián)的關(guān)鍵路徑,為高效、精準(zhǔn)地合成具有挑戰(zhàn)性的手性分子打開(kāi)了新的大門(mén)。

聲明:化學(xué)加刊發(fā)或者轉(zhuǎn)載此文只是出于傳遞、分享更多信息之目的,并不意味認(rèn)同其觀點(diǎn)或證實(shí)其描述。若有來(lái)源標(biāo)注錯(cuò)誤或侵犯了您的合法權(quán)益,請(qǐng)作者持權(quán)屬證明與本網(wǎng)聯(lián)系,我們將及時(shí)更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn